コレクション キレート滴定 計算 232197-キレート滴定 計算 亜鉛
Osaka Hightech Ac Jp
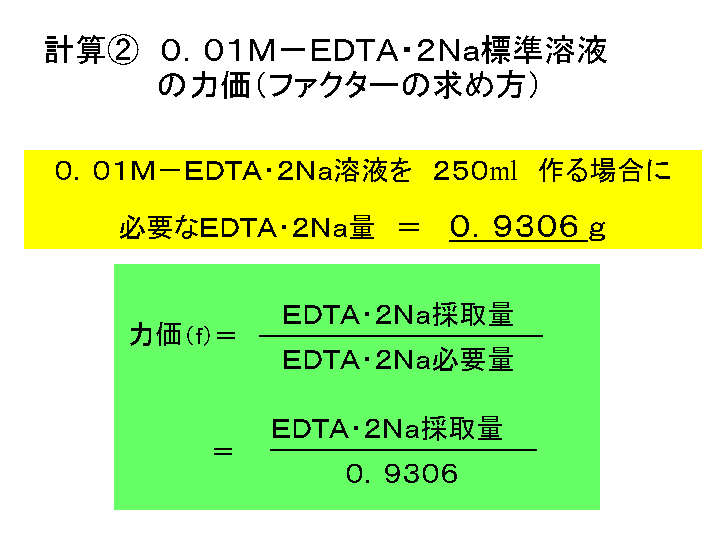
EDTA・2Naの必要量計算 1) 乾燥した空の秤量瓶の質量を分析天秤で測定する。 2) 秤量瓶に上皿天秤(電子天秤)を使って、EDTA・2Naを約0.9g採取する。 3) 分析天秤で、EDTA・2Naを入れK(βとも記載) = ( x ) / (x ・ (005 4x )^4 )となります。 この値が4 × 10^9であり、xについて解きましょう。 ただ、このまま解くと非常に難しい計算となるため、非常に小さ
キレート滴定 計算 亜鉛
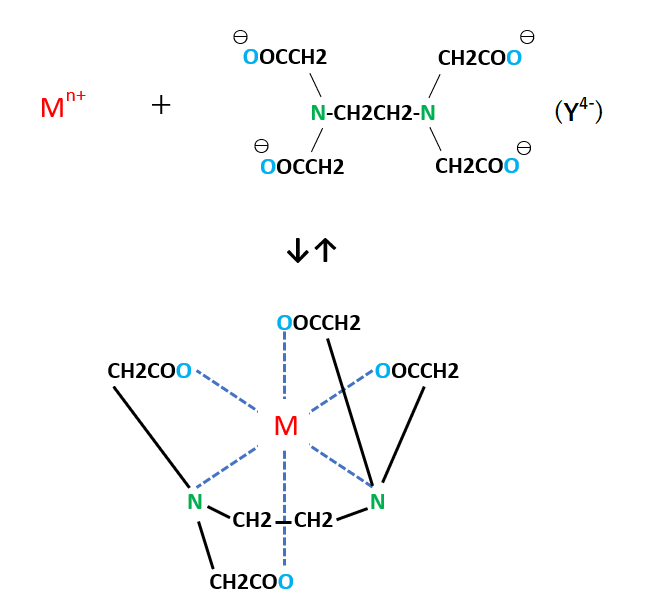
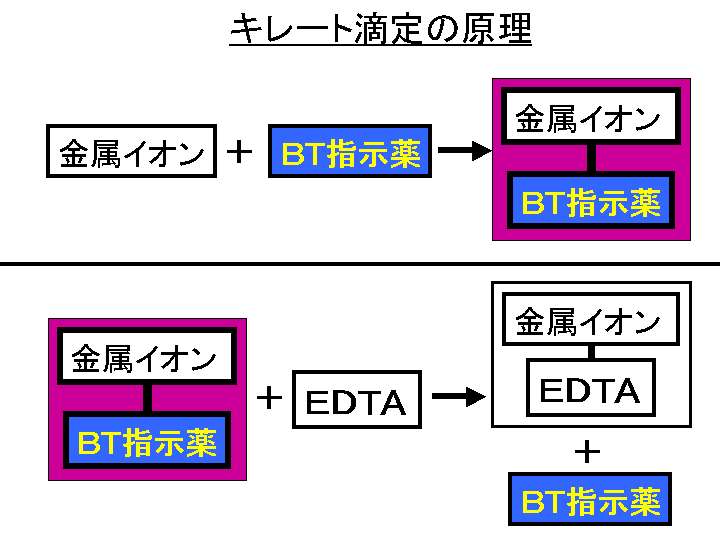
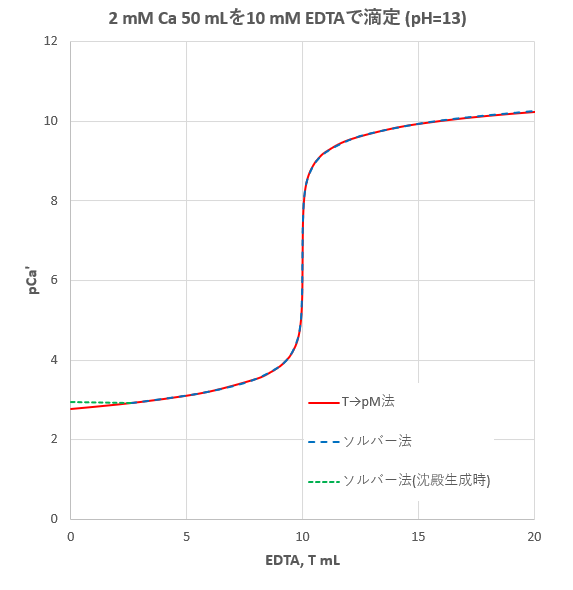
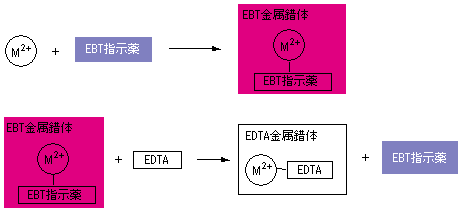
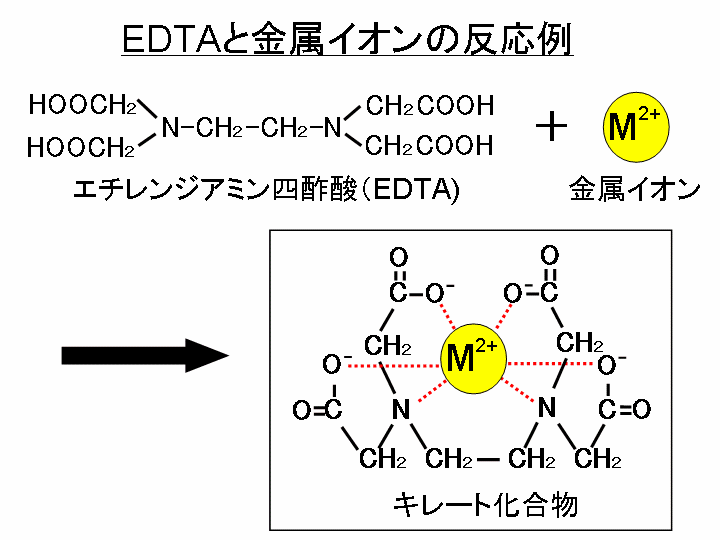
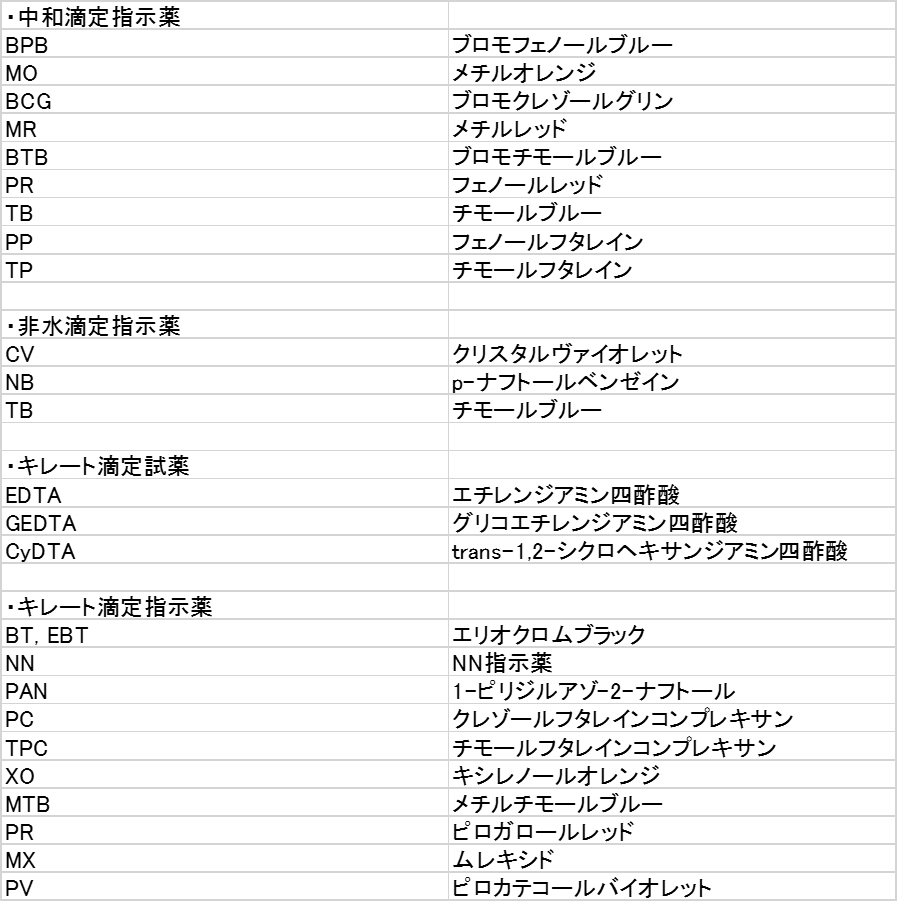
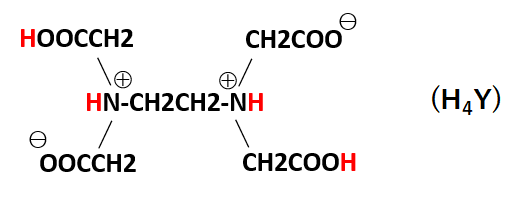
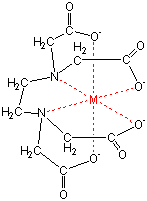
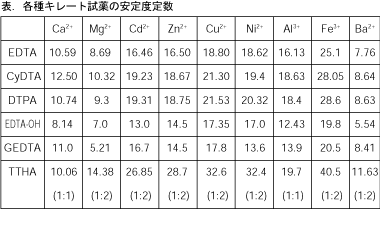
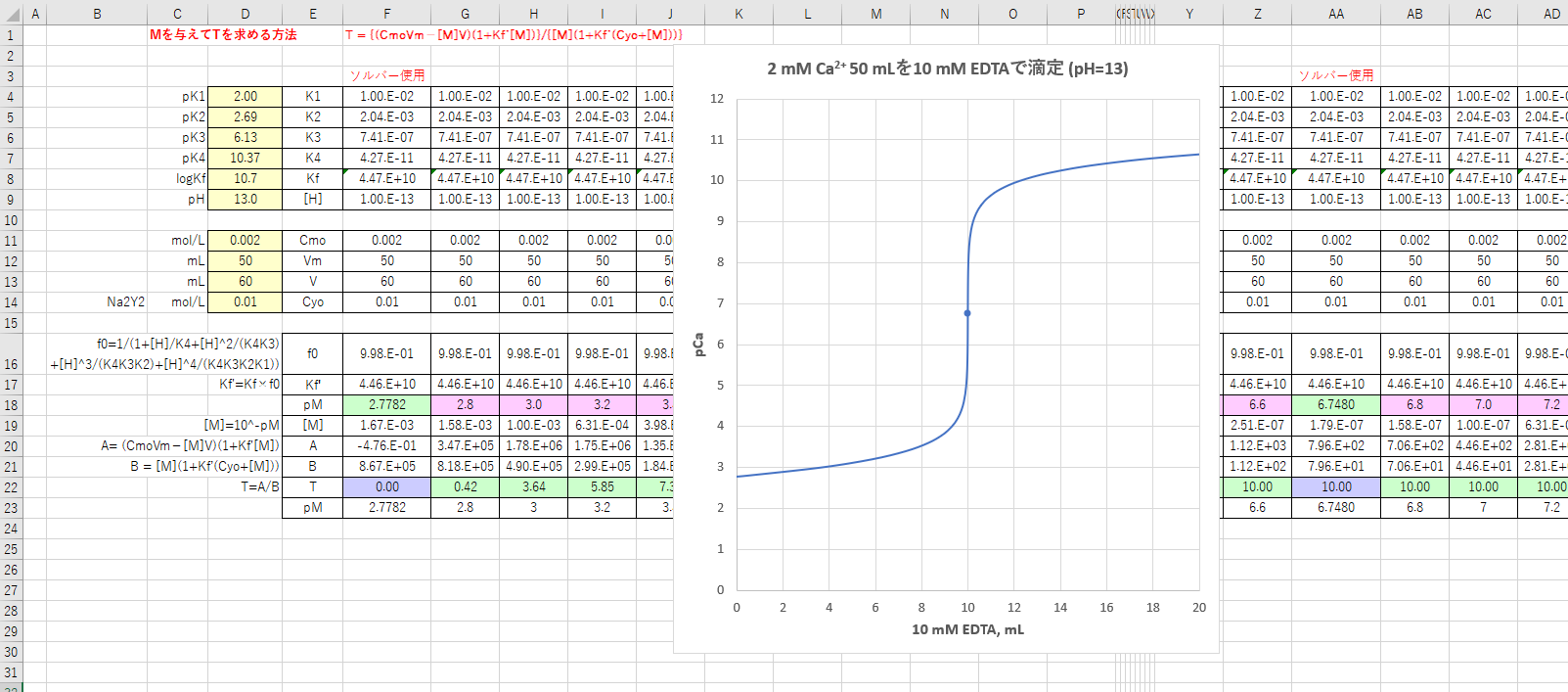
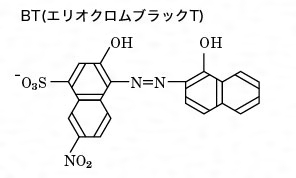
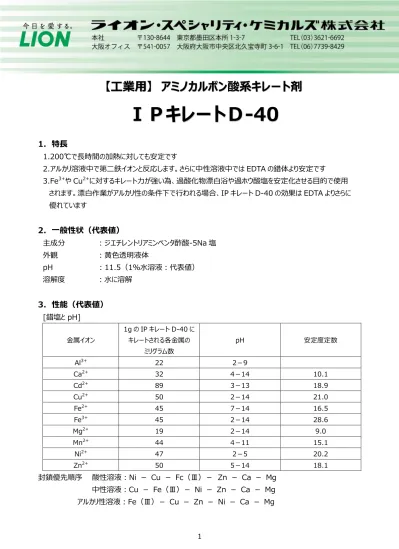
キレート滴定 計算 亜鉛-この滴定の原理は,エチレンジアミン四酢酸 (ethylendiaminetetraacetic acid,以下EDTA (図1))を用いた金属キレート錯体の形成であり,エリオクロムブラックT (以下EBT)という物質を指示薬とし6 キレート滴定法 に等しい*。 10K’ = CaY2 Ca2c Y = 50×103x x2 50×103 x2 = 18×10 上式から Ca2 = x = 527×107 M pCa = 628 (d)75 mL 滴下 過剰に加えられた滴定剤EDTA 濃度(c Y)はc Y = 0010×75 0010×50 50 75 = ×10 3 M であり,また CaY2 = 0010×50

京都大学 化学実験操作法 操作法 2 4 キレート滴定 Mg イオンの定量 Youtube
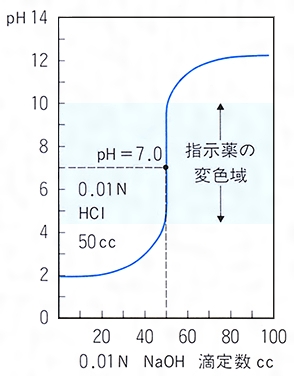
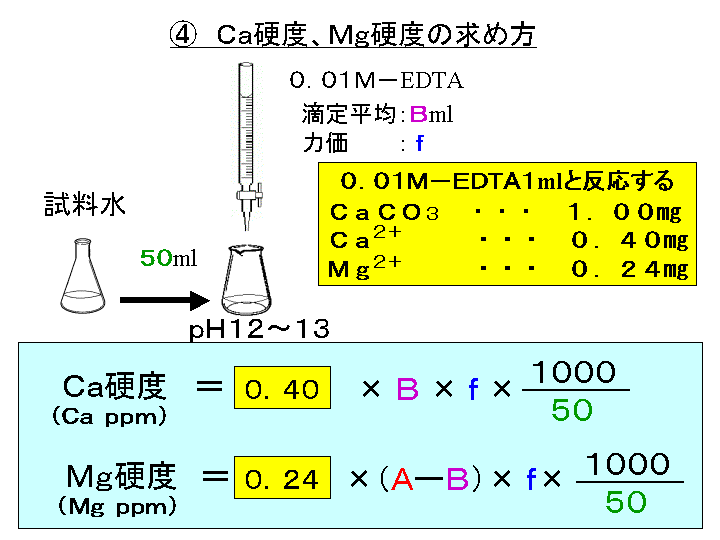
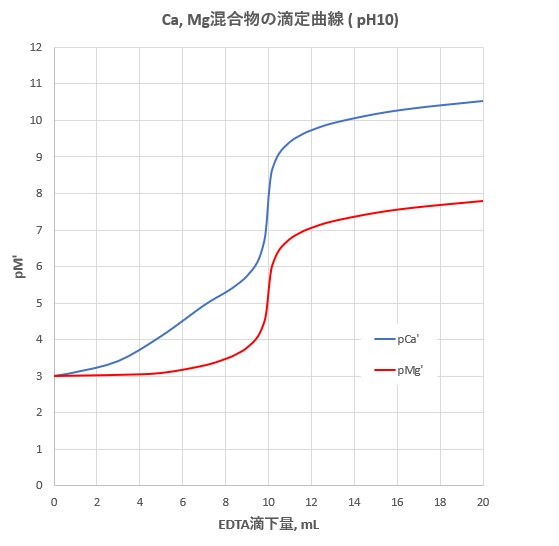
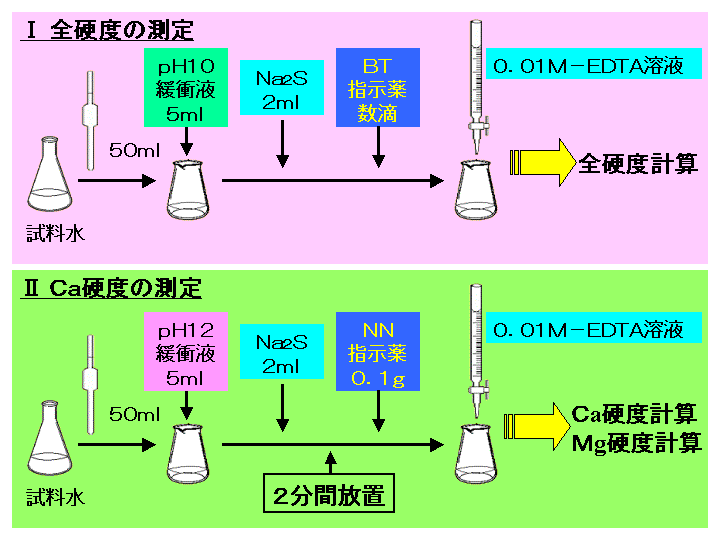
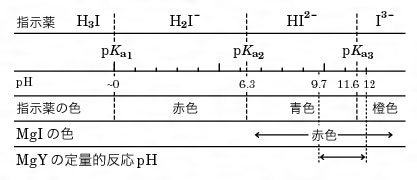
1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。 また、実験を通してキレート滴定法 の原理京都大学 全学共通教育 基礎化学実験ホームページ:http//wwwchemzenkyohkyotouacjp/化学実験操作法:操作法 2 4 キレートキレート滴定の基礎(4) 方法は逐次滴定というより,逆滴定に属するので次節 で詳論することとし,第一の方法について述べる。 低いph においてm 1をedta(yと略称)で滴定す る場合,yとhとの反
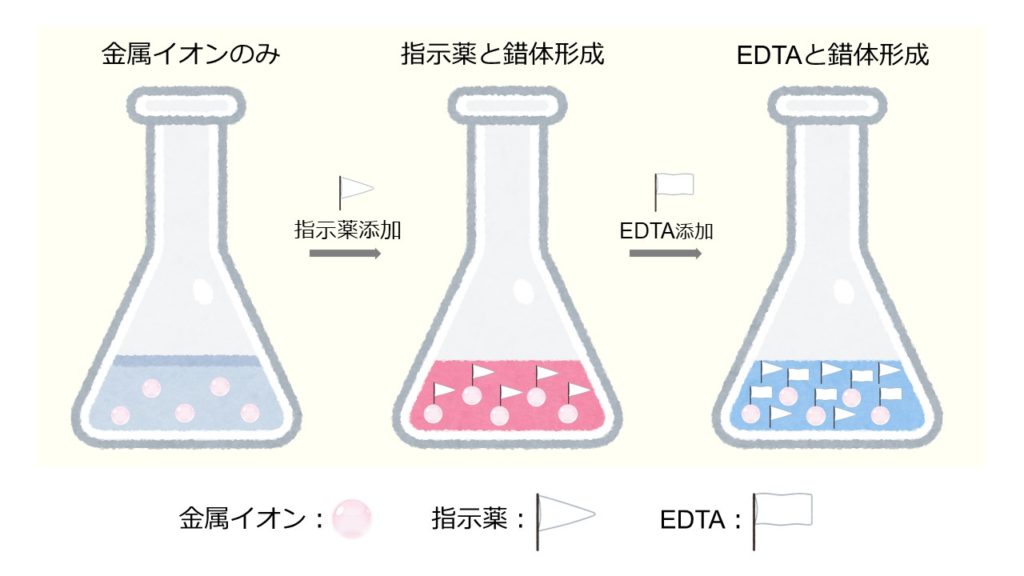
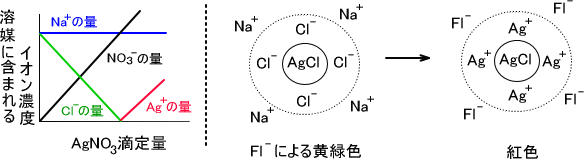
キレート滴定とは錯体の形成を利用して行う錯滴定 (compleximetric titration) の一種で、キレート試薬を用い、主に金属イオンを定量する分析法の1つとしてよく知られています。 主なキレート試 EDTA溶液の濃度(mol/l)×EDTA溶液の滴定値(ml)=Ca2とMg2の濃度の総和(mol/l)×試料量(ml) (式) × 3005 = x × 50 = 50x x = (mol/l) キレート滴定の濃度計算問題についてです。 解き方がわからないので、教えていただきたいです。 以下、問題内容です。 Ca2とMg2の混合
キレート滴定 計算 亜鉛のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 | ||
 | ||
 | ||
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 | ||
 |  | |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  | |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  | |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  | |
 |  | |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
 | ||
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  | |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 | ||
 |  |  |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 | ||
 | ||
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 | ||
 |  |  |
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 | ||
「キレート滴定 計算 亜鉛」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
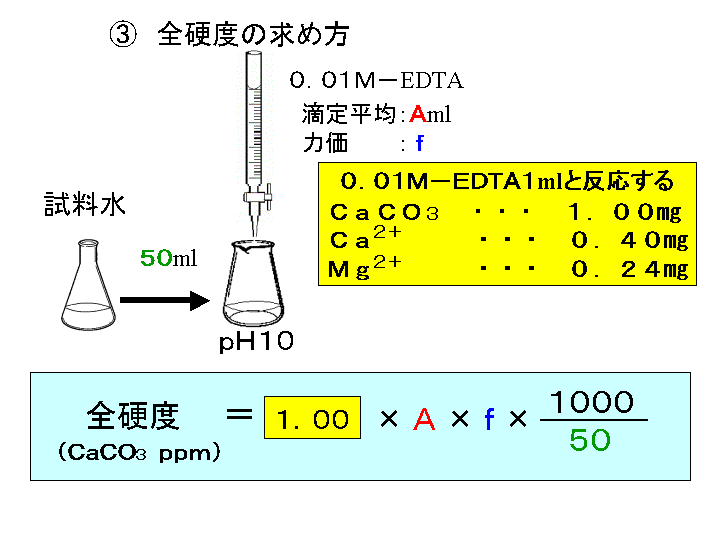
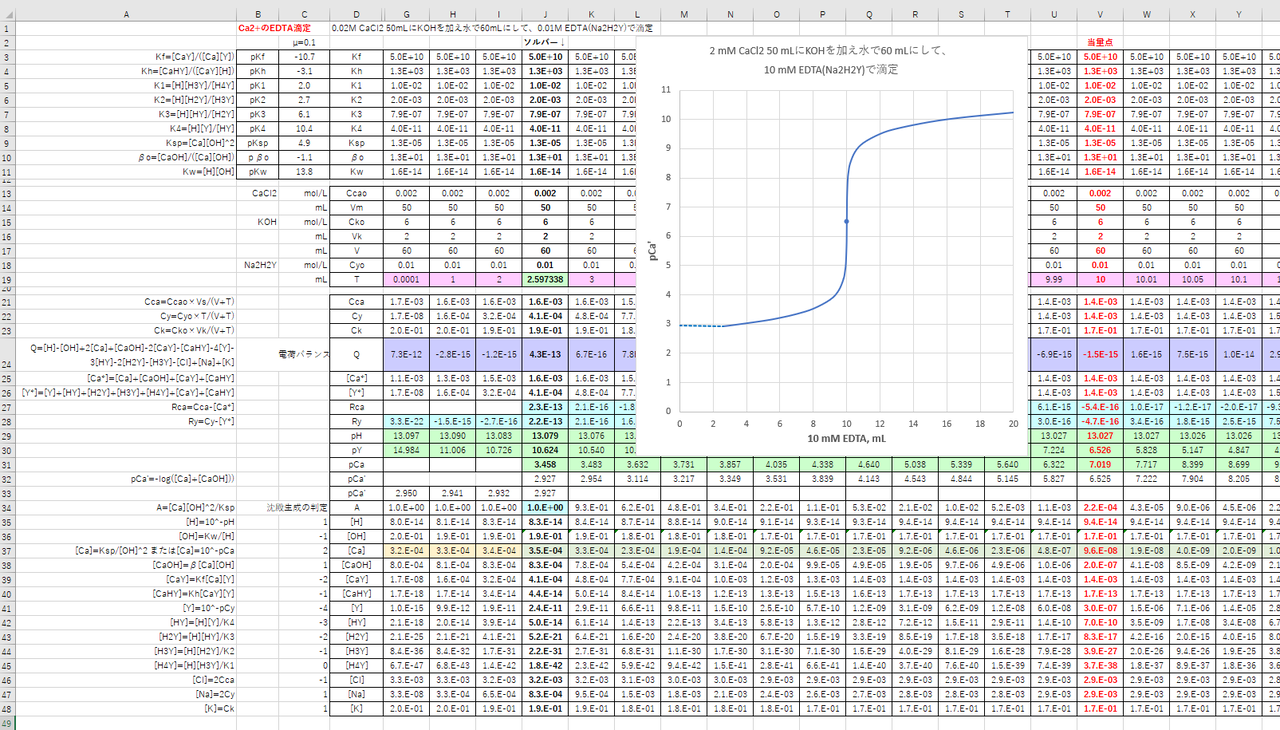
1000 H= a × I × )× f4) H:全硬度(mg CaCO3/L ) a :M/100 EDTA溶液の使用量(mL) I :検水(mL) f:M/100 EDTA溶液のファクター 検水採取量:50mL M/100 EDTA溶液の使用キレート滴定の計算方法 1 試薬の体積と初濃度 塩化アンモニウムNH 4 Cl-アンモニア水NH 3 系のpH緩衝液により,常にpH=10一定であると仮定する.計算を簡単化するために,カルシウムイオ
Incoming Term: キレート滴定 計算, キレート滴定 計算問題, キレート滴定 計算 亜鉛, キレート滴定 計算 銅, キレート滴定 計算式, キレート滴定 計算 カルシウム, キレート滴定 水の硬度 計算, キレート滴定 カルシウム マグネシウム 計算, キレート滴定 硬度 計算, edta キレート滴定 計算,
コメント
コメントを投稿